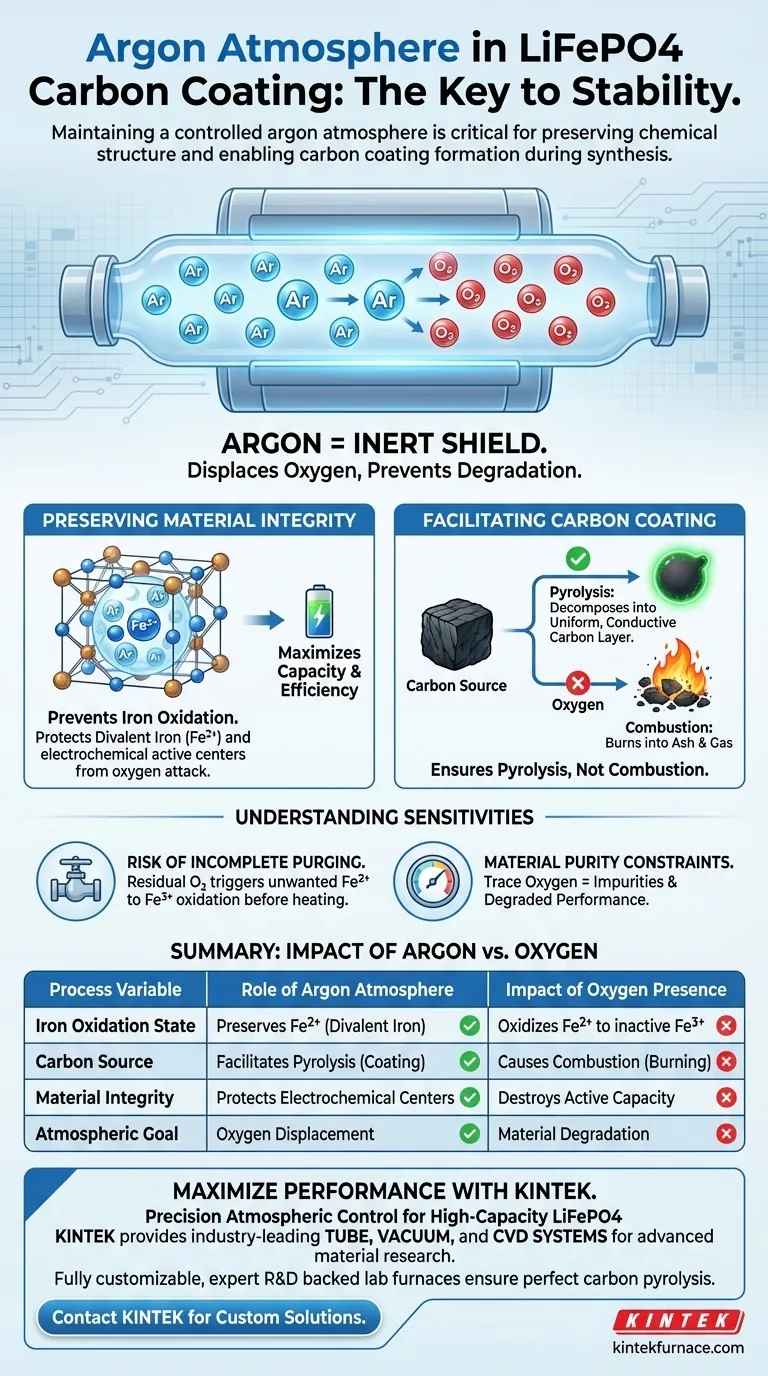
Le maintien d'une atmosphère d'argon contrôlée est le facteur le plus critique pour préserver la stabilité chimique lors de la synthèse du LiFePO4. Dans le contexte d'un four à tube de quartz, l'argon sert de bouclier inerte qui déplace l'oxygène atmosphérique. Cela empêche la dégradation de la structure chimique du matériau et permet au revêtement de carbone nécessaire de se former par décomposition thermique plutôt que par combustion.
En éliminant l'oxygène, l'argon préserve l'état essentiel de fer divalent (Fe2+) requis pour l'activité électrochimique et garantit que les sources de carbone subissent une pyrolyse plutôt qu'une combustion.

Préservation de l'intégrité du matériau
Prévention de l'oxydation du fer
La principale menace pour le LiFePO4 à haute température est la présence d'oxygène. Une atmosphère d'argon empêche efficacement l'oxydation du fer divalent (Fe2+) en fer trivalent (Fe3+).
Protection des centres actifs
Les performances du matériau de la batterie dépendent fortement de centres actifs électrochimiques spécifiques. Si le fer s'oxyde en raison d'un manque de gaz inerte, ces centres sont compromis, ce qui réduit considérablement la capacité et l'efficacité du matériau.
Facilitation du revêtement de carbone
Pyrolyse contre combustion
L'objectif du processus est de décomposer une source de carbone pour créer un revêtement conducteur. En présence d'oxygène, les sources de carbone combusteraient simplement, laissant des cendres ou des gaz plutôt qu'un revêtement utile.
Assurer une décomposition correcte
L'argon garantit que la source de carbone subit une pyrolyse. Ce processus permet au matériau organique de se décomposer chimiquement dans un environnement sans oxygène, déposant une couche de carbone uniforme et conductrice sur les particules de LiFePO4.
Comprendre les sensibilités du processus
Le risque d'un dégazage incomplet
Il ne suffit pas d'introduire de l'argon dans le tube de quartz ; le système doit être soigneusement purgé. Tout oxygène résiduel restant dans le tube avant le début du chauffage peut déclencher l'oxydation indésirable du Fe2+ en Fe3+.
Contraintes de pureté du matériau
Il n'y a pas de compromis en ce qui concerne le contrôle atmosphérique dans cette synthèse. Même des traces d'oxygène peuvent entraîner des impuretés qui dégradent la conductivité électronique et les performances globales de la cathode de batterie finale.
Assurer le succès de la synthèse
Pour obtenir un LiFePO4 de haute qualité, vous devez traiter le contrôle atmosphérique comme une variable de précision plutôt qu'un réglage passif.
- Si votre objectif principal est la pureté du matériau : Privilégiez le déplacement complet de l'oxygène pour maintenir strictement l'état d'oxydation Fe2+.
- Si votre objectif principal est la conductivité : Maintenez une pression continue et positive d'argon pour garantir que la source de carbone subisse une pyrolyse sans combustion.
Une atmosphère d'argon strictement contrôlée est la condition fondamentale pour convertir les précurseurs bruts en matériaux de batterie actifs électrochimiquement et performants.
Tableau récapitulatif :
| Variable de processus | Rôle de l'atmosphère d'argon | Impact de la présence d'oxygène |
|---|---|---|
| État d'oxydation du fer | Préserve le Fe2+ (fer divalent) | Oxyde le Fe2+ en Fe3+ inactif |
| Source de carbone | Facilite la pyrolyse (revêtement) | Provoque la combustion (brûlage) |
| Intégrité du matériau | Protège les centres électrochimiques | Détruit la capacité active |
| Objectif atmosphérique | Déplacement de l'oxygène | Dégradation du matériau |
Maximisez les performances de vos matériaux de batterie avec KINTEK
Le contrôle atmosphérique de précision fait la différence entre un LiFePO4 à haute capacité et une synthèse ratée. KINTEK fournit des systèmes de tubes, de vide et de CVD de pointe, spécialement conçus pour maintenir les environnements inertes rigoureux requis pour la recherche de matériaux avancés.
Soutenus par une R&D et une fabrication expertes, nos fours à haute température de laboratoire sont entièrement personnalisables pour répondre à vos besoins de traitement uniques, garantissant un déplacement complet de l'oxygène et une pyrolyse parfaite du carbone à chaque fois.
Prêt à améliorer la pureté de vos matériaux ? Contactez KINTEK dès aujourd'hui pour discuter de votre solution de four personnalisée.
Guide Visuel
Références
- Da Eun Kim, Yong Joon Park. Improving the Electrochemical Properties of LiFePO4 by Mixed-source-derived Carbon Layer. DOI: 10.33961/jecst.2025.00213
Cet article est également basé sur des informations techniques de Kintek Furnace Base de Connaissances .
Produits associés
- Four tubulaire à quartz de laboratoire Four tubulaire chauffant RTP
- 1200℃ Four à tube divisé Four à tube à quartz de laboratoire avec tube à quartz
- Four tubulaire vertical à quartz de laboratoire Four tubulaire
- Four tubulaire à quartz de laboratoire multizone Four tubulaire
- Four tubulaire sous vide à haute pression pour laboratoire Four tubulaire à quartz
Les gens demandent aussi
- Pourquoi un four tubulaire de laboratoire est-il nécessaire pour le processus de phosphuration ? Master Precision Material Synthesis
- Quel rôle joue un four tubulaire de laboratoire dans la recherche géologique et minéralogique ? Percez les secrets de la Terre avec précision
- Quelles conditions physiques un four tubulaire de laboratoire fournit-il pour les SOEC ? Chaleur de précision pour la caractérisation des solides.
- Quel rôle joue un système de four tubulaire de laboratoire dans la pyrolyse catalytique du LLDPE ? Amélioration du rendement et de la précision
- Pourquoi un four tubulaire de laboratoire est-il nécessaire pour la synthèse de BiVO4/RGO ? Obtenir un contrôle précis de la nano-structure



















