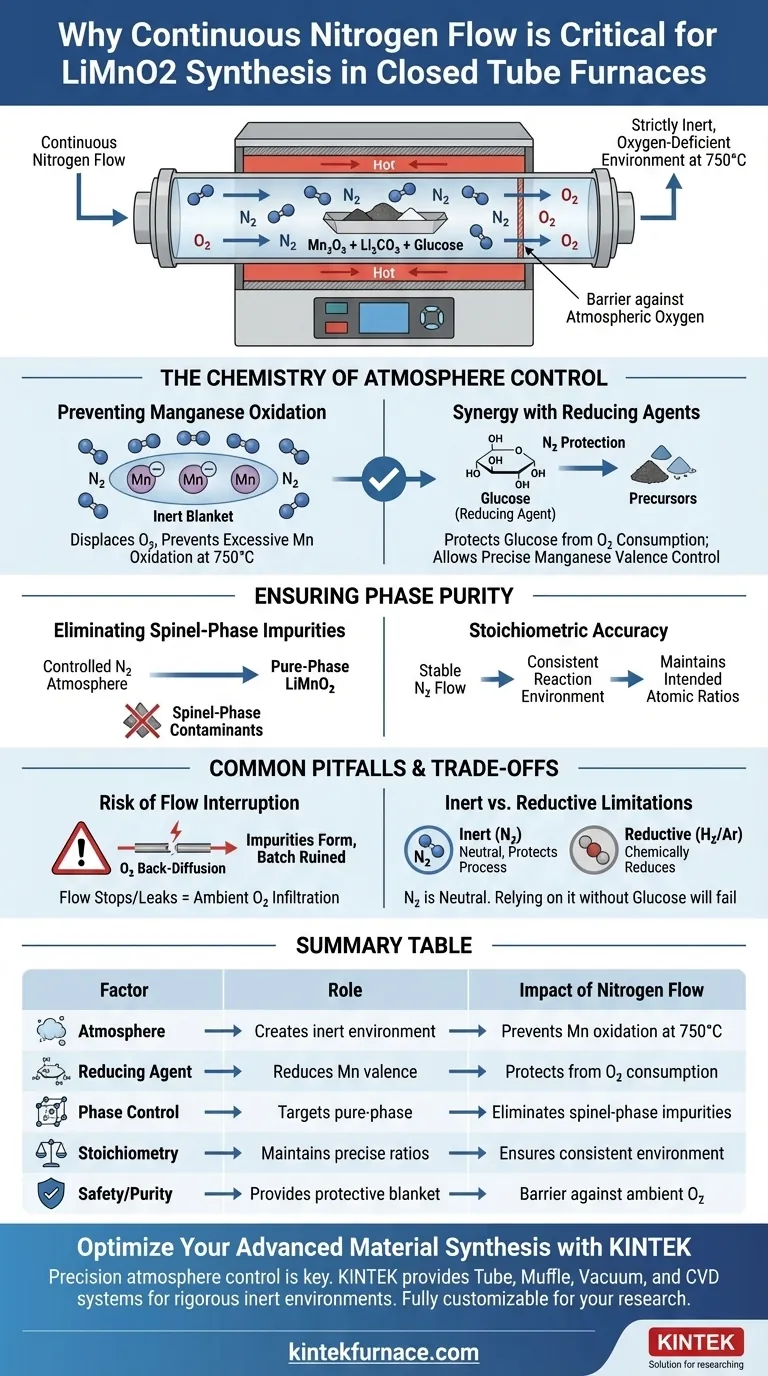
Un flux continu d'azote est essentiel pour créer un environnement strictement inerte et déficient en oxygène à l'intérieur du four tubulaire fermé. Cette atmosphère protectrice empêche l'oxydation excessive des ions manganèse pendant l'étape de synthèse à 750°C, assurant la formation réussie de LiMnO2 de phase pure.
La fonction principale du flux d'azote est d'agir comme une barrière contre l'oxygène atmosphérique. En maintenant un environnement déficient en oxygène, vous permettez à l'agent réducteur (glucose) de contrôler précisément l'état de valence du manganèse, empêchant la formation d'impuretés indésirables.

La chimie du contrôle atmosphérique
Prévention de l'oxydation du manganèse
À hautes températures, spécifiquement autour de 750°C, les ions manganèse sont très sensibles à une oxydation excessive s'ils sont exposés à l'air.
Le flux continu d'azote déplace l'oxygène à l'intérieur du tube, créant une "couverture" inerte autour des réactifs. Cette inhibition de l'oxydation est le prérequis fondamental pour synthétiser le bon matériau.
Synergie avec les agents réducteurs
L'azote seul fournit l'environnement inerte, mais la transformation chimique repose sur le glucose agissant comme agent réducteur.
L'atmosphère d'azote garantit que le glucose réagit exclusivement avec les matériaux précurseurs (Mn2O3 et Li2CO3). Il empêche le glucose d'être consommé par l'oxygène atmosphérique, préservant ainsi son pouvoir réducteur pour la synthèse de LiMnO2.
Assurer la pureté de phase
Élimination des impuretés de phase spinelle
Le risque principal dans cette synthèse est la formation de contaminants de phase spinelle, qui se produisent lorsque le manganèse est autorisé à sur-oxyder.
En contrôlant strictement l'atmosphère, le flux d'azote force la voie de réaction vers le lithium manganite de phase pure souhaité. Cette précision structurelle est vitale pour la performance électrochimique du matériau final.
Précision stœchiométrique
Pour que la réaction entre Mn2O3 et Li2CO3 donne la bonne stœchiométrie, les variables externes doivent être minimisées.
Un flux d'azote stable garantit que l'environnement de réaction reste constant tout au long du processus de chauffage. Cette stabilité permet aux précurseurs de réagir avec précision, en maintenant les rapports atomiques prévus dans le réseau cristallin final.
Pièges courants et compromis
Le risque d'interruption du flux
Le système repose sur un flux continu ; une atmosphère d'azote statique est souvent insuffisante.
Si le flux s'arrête ou si le tube n'est pas parfaitement scellé, l'oxygène ambiant peut diffuser dans la zone chaude. Même des traces d'oxygène à 750°C peuvent déclencher la formation d'impuretés, ruinant le lot.
Limitations inertes vs. réductrices
Il est important de distinguer une atmosphère inerte (azote) d'une atmosphère réductrice (comme H2/Ar utilisé pour d'autres précurseurs).
Dans cette synthèse spécifique, l'azote est neutre. Il ne réduit pas le manganèse lui-même ; il protège simplement le processus afin que le glucose ajouté puisse fonctionner efficacement. Compter sur l'azote sans l'agent réducteur correct ne produirait pas de LiMnO2.
Faire le bon choix pour votre objectif
Pour assurer le succès de votre synthèse en phase solide, alignez vos contrôles de processus sur vos exigences de pureté :
- Si votre objectif principal est la pureté de phase : Assurez-vous que le flux d'azote est actif avant le début du chauffage et continue jusqu'à ce que le four ait complètement refroidi pour éviter la ré-oxydation.
- Si votre objectif principal est la stœchiométrie : Vérifiez que votre concentration de glucose est calculée correctement, car l'atmosphère d'azote repose sur cet agent pour réduire chimiquement le manganèse.
Contrôlez rigoureusement l'atmosphère, et vous contrôlerez la qualité de votre précurseur final.
Tableau récapitulatif :
| Facteur | Rôle dans la synthèse de LiMnO2 | Impact du flux d'azote |
|---|---|---|
| Atmosphère | Crée un environnement inerte/déficient en oxygène | Prévient l'oxydation excessive de Mn à 750°C |
| Agent réducteur | Le glucose réduit la valence du manganèse | Protège le glucose de la consommation par l'oxygène atmosphérique |
| Contrôle de phase | Cible le lithium manganite de phase pure | Élimine la formation d'impuretés de phase spinelle |
| Stœchiométrie | Maintient des rapports atomiques précis | Assure un environnement de réaction et une stabilité constants |
| Sécurité/Pureté | Fournit une couverture de gaz protectrice | Agit comme une barrière contre la diffusion de l'oxygène ambiant |
Optimisez votre synthèse de matériaux avancés avec KINTEK
Le contrôle précis de l'atmosphère fait la différence entre le LiMnO2 de phase pure et les lots contaminés. KINTEK fournit des systèmes leaders de l'industrie de tubes, muffles, vide et CVD spécialement conçus pour maintenir les environnements inertes rigoureux requis pour la recherche et la production à enjeux élevés.
Soutenus par une R&D et une fabrication expertes, nos fours à haute température sont entièrement personnalisables pour répondre à vos exigences stœchiométriques et thermiques uniques. Ne laissez pas la contamination atmosphérique compromettre vos résultats.
Contactez KINTEK dès aujourd'hui pour personnaliser votre solution de synthèse
Guide Visuel
Références
- Jing Zhu, Run-Min Yao. Synthesis of Porous Lithium Ion Sieve with High Purity for Li+ Adsorption. DOI: 10.3390/ma18102373
Cet article est également basé sur des informations techniques de Kintek Furnace Base de Connaissances .
Produits associés
- Four tubulaire rotatif à fonctionnement continu sous vide scellé
- Four à creuset de condensation pour l'extraction et la purification du magnésium
- Four tubulaire CVD à chambre divisée avec machine CVD à station de vide
- 1200℃ Four à tube divisé Four à tube à quartz de laboratoire avec tube à quartz
- Four tubulaire sous vide à haute pression pour laboratoire Four tubulaire à quartz
Les gens demandent aussi
- Comment la quantité de matière traitée varie-t-elle entre les fours tubulaires rotatifs discontinus et continus ? Optimisez votre production efficacement
- Comment les fours à tube rotatif sont-ils utilisés dans la recherche en laboratoire ? Débloquez le traitement uniforme des poudres
- Quels sont les avantages techniques de l'utilisation d'un four tubulaire rotatif pour l'activation de l'hydrochar ? Atteindre une porosité supérieure
- Quels autres domaines utilisent les fours tubulaires rotatifs ? Découvrez des solutions de chauffage polyvalentes pour de multiples industries
- Quel est le but des fours tubulaires rotatifs ? Obtenir un traitement thermique uniforme pour les poudres et les granulés



















