L'hydrure de magnésium (MgH2) est préféré principalement pour ses capacités uniques de gestion thermique. Contrairement au magnésium métallique, la décomposition (déshydrogénation) du MgH2 est un processus endothermique. Cela permet au matériau d'agir comme un puits de chaleur interne pendant le traitement thermique, absorbant l'excès d'énergie et neutralisant efficacement les risques associés à la synthèse à haute température.
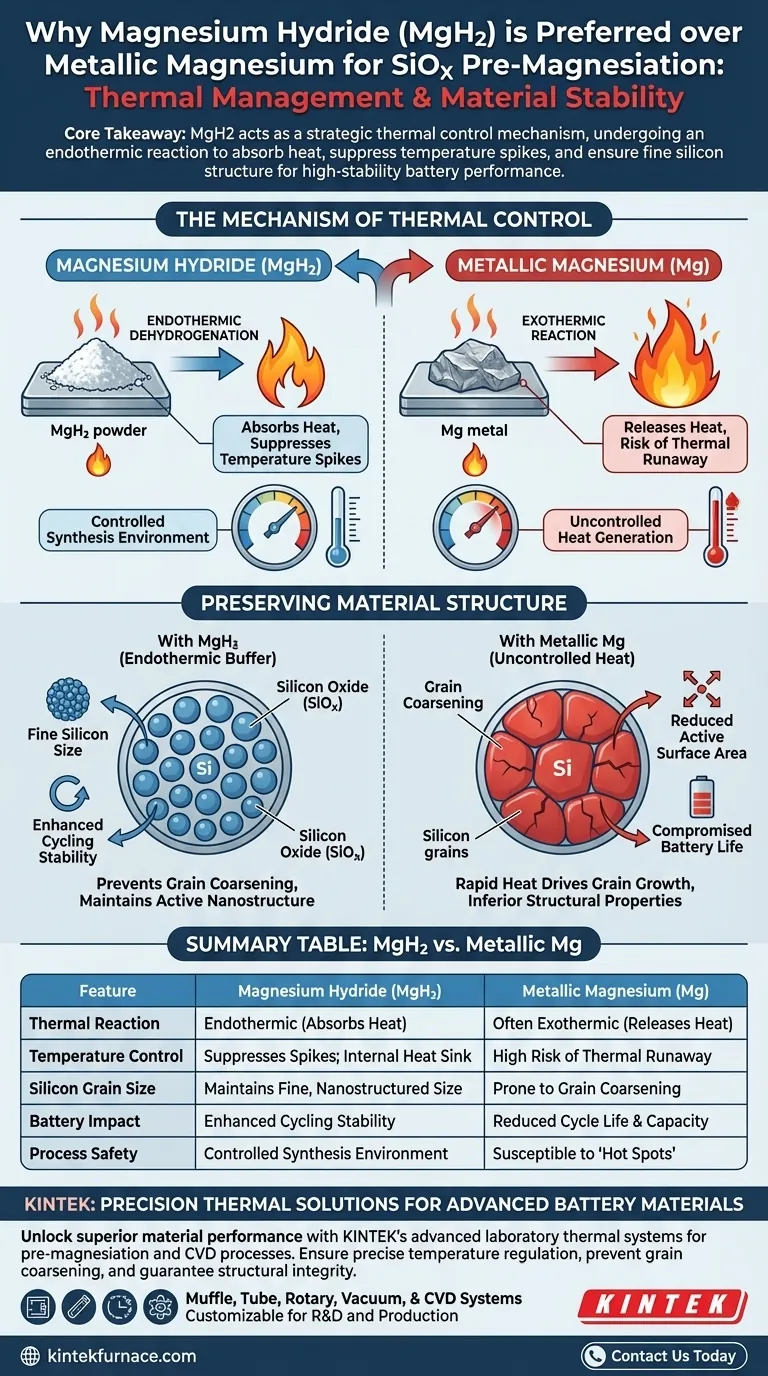
Point clé La sélection de l'hydrure de magnésium agit comme un mécanisme stratégique de contrôle thermique. En subissant une réaction endothermique, le MgH2 absorbe la chaleur pour supprimer les pics de température, empêchant le grossissement des grains de silicium et assurant l'intégrité structurelle fine requise pour des performances de batterie à haute stabilité.

Le mécanisme de contrôle thermique
Le rôle de la déshydrogénation endothermique
L'avantage fondamental du MgH2 réside dans sa réaction à la chaleur. Au fur et à mesure que le matériau subit un traitement thermique, il se décompose pour libérer de l'hydrogène.
Crucialement, cette décomposition est endothermique, ce qui signifie qu'elle consomme de la chaleur de l'environnement environnant. Cela contraste fortement avec les réactions exothermiques, qui libèrent de la chaleur et peuvent entraîner un emballement thermique ou des « points chauds » dans le mélange de matériaux.
Suppression des pics de température
Pendant le processus de pré-magnésiation, le maintien d'un profil de température stable est essentiel. L'absorption de chaleur fournie par le MgH2 supprime efficacement les pics de température intenses.
En modérant la température interne de la réaction, le MgH2 assure un environnement de synthèse contrôlé. Cela empêche l'accélération incontrôlable de la cinétique de réaction, ce qui est un risque courant lors de l'utilisation de réactifs qui n'offrent pas cet effet de tampon thermique.
Préservation de la structure du matériau
Prévention du grossissement des grains
Le contrôle de la température n'est pas seulement une caractéristique de sécurité ; il dicte la structure physique du matériau final. Les températures élevées provoquent généralement la fusion et la croissance des grains, un processus connu sous le nom de grossissement des grains.
Si la phase de silicium grossit, la surface active diminue et la capacité du matériau à accommoder les changements de volume pendant le cyclage de la batterie est compromise. Le MgH2 empêche cela en maintenant les températures sous contrôle.
Assurer une taille de grain de silicium fine
L'objectif de l'utilisation du MgH2 est de maintenir une taille fine du silicium actif.
En empêchant les pics thermiques qui entraînent la croissance, le silicium reste dans un état nanostructuré hautement actif. Cette structure fine est directement responsable de l'amélioration de la stabilité de cyclage du matériau d'anode SiOx résultant, conduisant à une batterie plus durable.
Les risques des sources alternatives
Réactions exothermiques incontrôlées
Bien que la référence principale souligne les avantages du MgH2, elle décrit implicitement les pièges de l'utilisation d'alternatives telles que le magnésium métallique sans mécanisme de tampon.
Sans le tampon endothermique du MgH2, l'environnement de réaction est sujet à une génération rapide de chaleur. Cette chaleur incontrôlée entraîne le grossissement des grains que les ingénieurs cherchent à éviter, résultant en un matériau de batterie aux propriétés structurelles inférieures et à la durée de vie du cycle réduite.
Faire le bon choix pour votre objectif
Lors de la conception de protocoles de synthèse pour les anodes d'oxyde de silicium, le choix du précurseur dicte la qualité de l'architecture finale.
- Si votre objectif principal est la stabilité de cyclage : Privilégiez le MgH2 pour maintenir la taille fine des grains de silicium nécessaire à une endurance à long terme.
- Si votre objectif principal est le contrôle du processus : Utilisez le MgH2 pour agir comme un tampon thermique interne, atténuant le risque de pics de température pendant le traitement thermique.
Contrôlez la température au niveau microscopique, et vous contrôlez les performances de la cellule finale.
Tableau récapitulatif :
| Caractéristique | Hydrure de magnésium (MgH2) | Magnésium métallique (Mg) |
|---|---|---|
| Réaction thermique | Endothermique (Absorbe la chaleur) | Souvent exothermique (Libère de la chaleur) |
| Contrôle de la température | Supprime les pics ; puits de chaleur interne | Risque élevé d'emballement thermique |
| Taille des grains de silicium | Maintient une taille fine et nanostructurée | Sujet au grossissement des grains |
| Impact sur la batterie | Stabilité de cyclage améliorée | Durée de vie et capacité de cyclage réduites |
| Sécurité du processus | Environnement de synthèse contrôlé | Sujet aux « points chauds » |
Solutions thermiques de précision pour les matériaux de batterie avancés
Libérez des performances matérielles supérieures avec les systèmes thermiques de laboratoire avancés de KINTEK. Que vous effectuiez une pré-magnésiation de SiOx ou des processus CVD complexes, notre équipement assure la régulation précise de la température nécessaire pour prévenir le grossissement des grains et assurer l'intégrité structurelle.
Soutenue par une R&D et une fabrication expertes, KINTEK propose des systèmes Muffle, Tube, Rotatif, sous Vide et CVD haute performance, tous personnalisables selon vos besoins spécifiques de recherche ou de production.
Prêt à stabiliser votre processus de synthèse ? Contactez-nous dès aujourd'hui pour consulter nos experts et trouver la solution haute température parfaite pour votre laboratoire.
Guide Visuel
Références
- Hyunsik Yoon, Hansu Kim. Magnesiated Si‐Rich SiO<sub><i>x</i></sub> Materials for High‐Performance Lithium‐Ion Batteries. DOI: 10.1002/batt.202500473
Cet article est également basé sur des informations techniques de Kintek Furnace Base de Connaissances .
Produits associés
- Éléments chauffants thermiques en disiliciure de molybdène MoSi2 pour four électrique
- Four à creuset de condensation pour l'extraction et la purification du magnésium
- Four à atmosphère inerte contrôlée d'azote et d'hydrogène
- Four tubulaire PECVD coulissant avec machine PECVD à gazéifieur de liquide
- Four tubulaire à quartz de laboratoire Four tubulaire chauffant RTP
Les gens demandent aussi
- Quelle est la durée de vie des éléments chauffants en MoSi2 et comment se comportent-ils dans les environnements chimiques ? Maximisez la longévité grâce à une utilisation appropriée
- Quelles sont les applications des éléments chauffants en disiliciure de molybdène ? Atteindre une stabilité thermique extrême pour les processus industriels
- Quelles sont les propriétés du disiliciure de molybdène (MoSi2) qui le rendent adapté aux applications à haute température ? Découvrez sa résilience à haute température
- Quels types d'applications industrielles conviennent le mieux aux éléments chauffants en MoSi2 ? Maximiser la stabilité à haute température
- Quelles sont les caractéristiques des éléments chauffants au disiliciure de molybdène ? Débloquez les performances à haute température

















