L'exceptionnelle résistance chimique du carbure de silicium (SiC) dans les fours industriels provient d'une combinaison de sa structure atomique inhérente et de sa capacité à former un bouclier protecteur en surface. À la base, la liaison covalente incroyablement forte entre les atomes de silicium et de carbone nécessite une énergie immense pour être rompue. Ceci est complété par une couche passive auto-génératrice de dioxyde de silicium (SiO₂) qui se forme à sa surface, l'isolant efficacement de l'environnement.
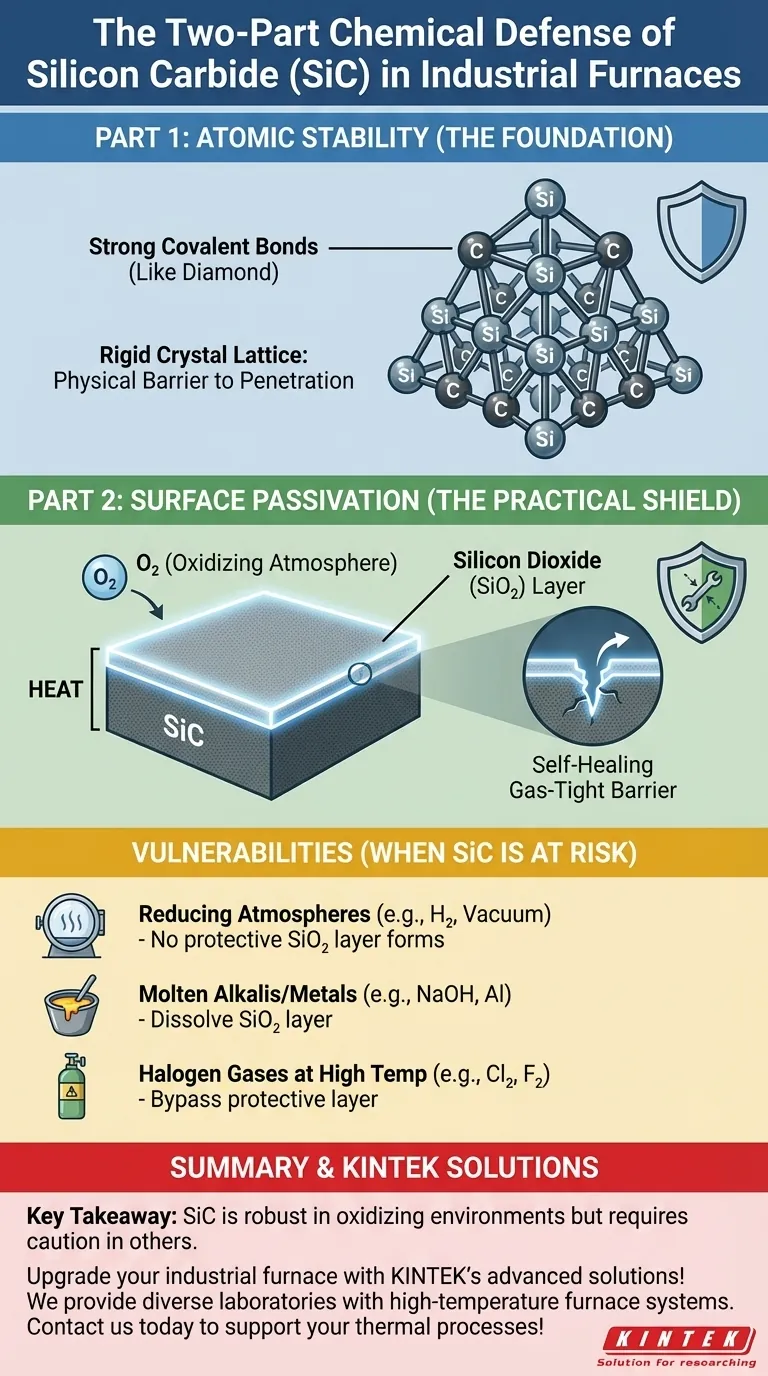
La durabilité du carbure de silicium n'est pas une propriété unique, mais un système de défense en deux parties. Sa force fondamentale provient de ses liaisons atomiques stables, tandis que sa résilience pratique dans les fours provient d'une fine couche de verre (dioxyde de silicium) auto-cicatrisante qui se forme à sa surface à hautes températures.

Le Fondement : Stabilité Atomique
La racine de la résilience du SiC réside dans sa configuration atomique. Contrairement aux métaux, qui sont maintenus ensemble par une "mer" d'électrons lâche, les atomes de SiC sont enfermés dans une structure rigide et puissante.
La Force de la Liaison Covalente
Les atomes de silicium et de carbone partagent des électrons dans une forte liaison covalente. Ce type de liaison est l'un des plus stables en chimie, similaire aux liaisons qui confèrent au diamant sa dureté légendaire. Rompre cette liaison nécessite une quantité significative d'énergie, rendant le SiC intrinsèquement non réactif dans la plupart des conditions.
La Structure Cristalline Rigide
Ces liaisons fortes arrangent les atomes dans un réseau cristallin tétraédrique très compact. Cette structure rigide laisse très peu de place aux atomes étrangers ou aux molécules corrosives pour pénétrer le matériau et initier une réaction chimique. Elle crée une barrière physique au niveau atomique.
Le Bouclier Pratique : Passivation de Surface
Bien que la stabilité atomique soit le fondement, la véritable clé de la performance du SiC dans les fours est sa capacité à se protéger. Ce processus est connu sous le nom de passivation.
Formation de la Couche de Dioxyde de Silicium (SiO₂)
Lorsque le carbure de silicium est chauffé dans une atmosphère contenant de l'oxygène (comme l'air), le silicium à la surface réagit avec l'oxygène. Cette réaction forme une couche mince, dense et très stable de dioxyde de silicium (SiO₂), qui est essentiellement une forme de quartz ou de verre.
Comment Fonctionne la Couche Protectrice
Cette couche de SiO₂ est non poreuse et adhère fortement au substrat de SiC. Elle agit comme une barrière étanche aux gaz, séparant physiquement le carbure de silicium sous-jacent des gaz réactifs du four. Si la couche est rayée ou endommagée à hautes températures, le SiC exposé réagira simplement avec plus d'oxygène pour "cicatriser" le bouclier, ce qui en fait une défense remarquablement efficace et renouvelable.
Comprendre les Compromis : Quand le SiC est Vulnérable
Aucun matériau n'est parfait, et comprendre les limitations du SiC est essentiel pour une application appropriée. Sa résistance chimique dépend fortement de l'environnement du four.
Le Rôle de l'Atmosphère
La couche protectrice de SiO₂ ne se forme que dans une atmosphère oxydante. Dans une atmosphère réductrice (comme l'hydrogène pur ou un vide poussé), cette couche ne peut pas se former ou peut être éliminée. Cela rend le SiC plus vulnérable à la réaction avec d'autres matériaux.
Attaque par les Alcalis et Métaux Fondus
La couche de SiO₂, bien que résistante aux acides, peut être dissoute par des alcalis fondus forts (comme l'hydroxyde de sodium) et certains métaux fondus (comme l'aluminium). Une fois cette couche protectrice disparue, ces produits chimiques agressifs peuvent attaquer directement le carbure de silicium lui-même.
Gaz Halogènes à Hautes Températures
À très hautes températures, les gaz halogènes comme le chlore et le fluor sont suffisamment réactifs pour contourner la couche protectrice et attaquer le SiC, formant des halogénures de silicium volatils. Il s'agit d'un mode de défaillance spécifique à prendre en compte dans les applications de traitement chimique.
Application à Votre Environnement de Four
Votre choix de matériau doit être aligné avec les conditions chimiques de votre processus. Comprendre le mécanisme de défense du SiC vous permet de prédire ses performances et d'assurer l'intégrité du processus.
- Si votre objectif principal est un fonctionnement à haute température dans l'air ou une atmosphère oxydante : Le SiC est un excellent choix, car l'environnement renforce continuellement la couche protectrice de SiO₂ qui assure sa longévité.
- Si votre objectif principal est de travailler avec des alcalis fondus (caustiques) ou des métaux réactifs : Le SiC est probablement un mauvais choix, car ces matériaux détruiront sa couche protectrice et provoqueront une dégradation rapide.
- Si votre objectif principal est de fonctionner sous vide poussé ou dans une atmosphère réductrice : Le SiC reste structurellement stable, mais vous perdez le bénéfice du bouclier d'oxyde auto-cicatrisant, ce qui doit être pris en compte dans les calculs de durée de vie et de contamination.
En comprenant à la fois la force intrinsèque et les dépendances environnementales du carbure de silicium, vous pouvez concevoir en toute confiance un processus thermique plus fiable et efficace.
Tableau Récapitulatif :
| Facteur | Rôle dans la Résistance Chimique |
|---|---|
| Structure Atomique | Les liaisons covalentes fortes et le réseau cristallin rigide résistent à la pénétration et aux réactions |
| Passivation de Surface | Forme une couche protectrice de SiO₂ dans les atmosphères oxydantes, auto-cicatrisante si endommagée |
| Dépendances Environnementales | Vulnérable dans les atmosphères réductrices, les alcalis fondus et les gaz halogènes à hautes températures |
Améliorez votre four industriel avec les solutions avancées de KINTEK ! Grâce à une R&D exceptionnelle et une fabrication interne, nous fournissons à divers laboratoires des systèmes de fours à haute température tels que les fours à moufle, tubulaires, rotatifs, sous vide et à atmosphère contrôlée, ainsi que des systèmes CVD/PECVD. Notre capacité de personnalisation approfondie garantit un ajustement précis à vos besoins expérimentaux uniques, améliorant la durabilité et l'efficacité. Contactez-nous dès aujourd'hui pour discuter de la manière dont nous pouvons soutenir vos processus thermiques !
Guide Visuel
Produits associés
Les gens demandent aussi
- Quels sont les types courants d'éléments chauffants en carbure de silicium ? Explorez les formes, les revêtements et les performances à haute température
- Quelles sont les principales caractéristiques des éléments chauffants en carbure de silicium par rapport aux éléments chauffants métalliques ? Découvrez les différences clés pour vos besoins à haute température
- Quelles sont les propriétés uniques des éléments chauffants en carbure de silicium ? Avantages clés pour les performances à haute température
- Quels sont les avantages opérationnels des éléments chauffants en carbure de silicium ? Atteindre l'efficacité et la durabilité à haute température
- Quelles sont les capacités de température et les options de montage des éléments chauffants en carbure de silicium ? Libérez une flexibilité et une durabilité à haute température
